
Bu yazının içinde neler var?
Atomlar hem maddenin hem de evrenin temel yapı taşlarıdır. Evren gibi çok büyük makro ölçeği ve atom gibi mikro ölçeği kavramak insanlar için her zaman zor olmuştur. Akıl almaz mesafeler ve mikroskoplarla dahi tespit edilmesi güç küçük yapılar henüz insanlığın tam olarak anlayamadığı birçok sırrı barındırır. Ancak evrende nereye bakarsak bakalım atomların varlığını görürüz.
Atomların maddenin bölünemeyen en küçük yapı taşı olduğu varsayımlarından bugün proton, nötron ve elektronları meydana getiren kuark ve leptonların varlığı bilinirken daha da küçük yapı taşları olabilecek sicimlerden söz edilmektedir. Atomaltı parçacıklar olarak adlandırılan bu kuark ve leptonlar bir araya gelerek elektron, proton ve nötronları oluşturur. Örneğin, iki yukarı kuark ve bir aşağı kuark protonları oluştururken iki aşağı ve bir yukarı kuark nötronları meydana getirir (energy.gov, 2022). Üstelik bu kadar küçük ölçekte klasik fizik kurallarının geçerliliğini kaybettiği ve kuantum mekaniğinin devreye girdiği gibi oldukça heyecan verici gelişmeler de elde edilmiştir.
Dilerseniz gelin öncelikle atomun nasıl tanımlandığına ve tarih boyunca atom fikrinin dönüşümüne göz atalım.
Atom Nedir?
Maddenin en küçük yapı taşı olarak da bilinen atomlar, bir kimyasal elementin karakteristik özelliklerine sahip olan en küçük birimidir. Atomun boyutu 1 Angstrom ile ifade edilir. Bu da metrenin metrenin 10 milyarda 1’ine gelen bir değerdir. Canlı yaşamı için gerekli olan su molekülünü ele alırsak, hidrojen ve oksijen atomlarından meydana geldiğini görürüz. Oksijen ve hidrojen aynı zamanda birer elementtir.
Periyodik tabloda yer alan elementler tek cins atomdan meydana gelmiş olan saf maddelerdir. Bir elementin atomu her zaman aynı sayıda proton barındırır. Elementlerin kendilerine özgü olan bu özelliği proton sayısının aynı zamanda atom numarası olarak da kullanılır. Elementler sahip oldukları atom numarasına göre periyodik tabloda konumlandırılır.
Atom Yapısı Nelerden Oluşur?
Oldukça küçük yapıdaki atomların içerisinde proton, nötron ve elektronlar olmak üzere üç farklı atomaltı parçacık bulunur. Bu atomaltı parçacıklar da kuark ve lepton olarak adlandırılan daha da küçük yapılardan meydana gelir. Atomların, bu parçacıkların dışında kalan büyük bir kısmı ise boşluktan ibarettir.
Atomların çekirdeğinde nötr yani yüksüz nötronlar ve pozitif yüklü protonlar bulunur. Geneline bakıldığında atomun çekirdeği pozitif yüke sahiptir. Bu pozitif yüklü çekirdeğin etrafında ise yörüngelere dağılmış negatif yüklü elektronlar yer alır.
Çekirdekte yer alan proton sayısı bir element için asla değişmezken nötron sayısı değişiklik gösterir. Bir elementin farklı sayıda nötron içeren atomları izotop olarak adlandırılır. Elementlerin birden fazla farklı izotopu bulunabilir. İzotop hali elementin doğal halinden farklı olarak radyoaktiflik gibi özellikler gösterebilir.
Nört bir atomun çekirdeğinde yer alan proton sayısı kadar elektronu bulunur. Bu sebeple yük bakımından dengededir. Atomların çarpışmaları veya kimyasal reaksiyona girmeleri elektron kazanmalarına veya kaybetmelerine neden olur. Elektron alışverişi süreci iyonlaşma olarak adlandırılır. Elektron kaybetmiş veya kazanmış atomlara ise iyon denir. Elektron kaybeden bir atomda pozitif yük çoğunlukta olduğundan pozitif iyon, elektron alan atomda ise negatif yük daha fazla olduğundan negatif iyon olarak adlandırılır.
Atom'u Kim Buldu? Atom'un Tarihçesi

Maddenin oldukça küçük parçacıklardan meydana geldiği düşüncesi M.Ö. 5. Yüzyıl Yunan filozoflarına kadar dayanır. Demokritos’a göre madde sonsuza kadar bölünebilecek bir yapıdan ziyade bir noktada sonlanan ve sonuçta parçalanamaz bir parça barındırır yapıdaydı. Bu düşüncesinden yola çıkan Demokritos bu bölünemeyen yapı taşı için Yunanca bölünemeyen anlamını taşıyan “atomos” kelimesini kullanmıştır.
18. Yüzyılın sonları ve 19. Yüzyılın başlarına gelindiğinde ise atom üzerine bilimsel çalışmalar hız kazanmıştır. Atom konusuna bilimsel olarak yaklaşan ilk kişi oluşturduğu atom modeli ile John Dalton’dur. Bilim dünyasının ilgisini yeniden bu yöne çekmeyi başaran Dalton’un modeli defalarca yanlışlansa da sonraki çalışmalara yol gösterdiği için son derece önemlidir.
Takip eden yıllarda JJ Thomson, Ernest Rutherford, Niels Bohr, Erwin Schrödinger gibi bilim insanlarının çalışmaları ile günümüz modern atom modeline ulaşılmıştır.
Atom Modelleri ve Özellikleri
Antik Yunan filozofları tarafından maddeyi meydana getiren yapı taşları hakkındaki ilk düşüncelerden bu yana atomlar konusunda onlarca fikir ortaya atılmıştır. 1800’lü yıllardan günümüze kadar geçen süre içerisinde ise atomlara bilimsel açıdan yaklaşarak bilim insanları tarafından çeşitli teoriler ortaya atılmıştır.
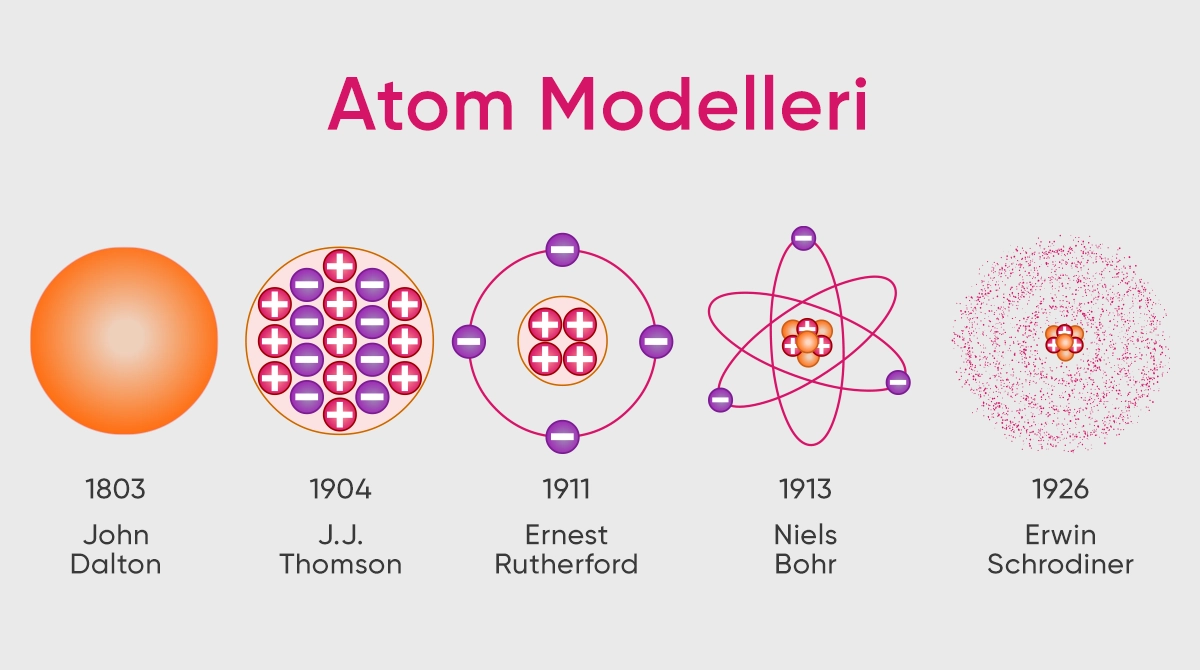
Dalton Atom Modeli
John Dalton tarafından 1803 yılında ortaya atılan atom modeli, bilimsel bir yaklaşım olmasından dolayı ilk atom teorisi olarak kabul edilir. Dalton’un teorisine göre maddenin en küçük yapıtaşı atom adı verilen küçük ve bölünemez parçacıklardır.
Dalton’un teorisine göre bu atomlar adeta birer bilardo topu gibi katı bir yapıya sahiptir. Hareket halindeki bu atomlar birbirleri ile çarpışarak etkileşime girer ve kimyasal reaksiyonlara sebep olurlar.
Atom’un iç yapısını açıklama konusunda yetersiz kalan bu teorinin ilerleyen yıllarda gerçekleşen bilimsel gelişmeler ile atomun parçalanamadığı yönündeki görüşü gibi pek çok yönden yetersiz olduğunu ortaya koymuştur.
JJ Thomson Atom Modeli
John Dalton’un atom modelinden 100 yıl sonra ise JJ Thomson’ın 1904 yılında ortaya koyduğu atom modelinde, atomların pozitif yüklü bir ortam olduğu ve içerisinde negatif yüklü elektronların varlığını öne sürmüştür. Bu model üzümlü kek modeli olarak da bilinir. Atom pozitif yüklü bir kek gibi düşünülebilirken negatif yüklü elektronlar ise adeta birer üzüm gibi atomun içine gömülü üzümler gibidir.
Thomson çalışmaları atom altı parçacıklardan biri olan elektronların keşfi açısından son derece önemlidir. Katot ışınları ile gerçekleştirdiği çalışmalar sonucunda negatif yüklü parçacıklar olan elektronları keşfeden Thomson, atomların eşit miktarda pozitif yüke sahip olarak nötr bir yapıda olması gerektiğini savunmuştur.
Modelin eksik kaldığı noktalar ise, atomun kararlılığı, radyoaktivite, izotoplar gibi konuları açıklayamaması ve protonların varlığını hesaba katmamasıdır.
Rutherford Atom Modeli
Atom üzerine bilim dünyasının çalışmaları son sürat devam bir dönemde, 1911 yılında Ernest Rutherford, gezegen modeli olarak da bilinen kendi atom modelini ortaya koymuştur. Rutherford gerçekleştirdiği deneylerde ince altın folyo tabakasına, pozitif yüklü parçacıklar yollamıştır. Parçacıkların büyük bir kısmı folyodan düz bir şekilde geçerken az bir kısmı ise büyük açılarla saptığını tespit etmiştir.
Gerçekleştirdiği çalışmalar neticesinde, atomların merkezde yoğun ve küçük pozitif yüklü çekirdeğe sahip olduğu sonucuna varmıştır. Buna ek olarak çekirdek etrafında adeta güneşin etrafında dönen gezegenler gibi negatif yüklü elektronların olduğunu varsayılmıştır.
Rutherford modeli ise elektronların dalga benzeri yapılarını hesaba katmıyordu. Buna ek olarak negatif yüklü elektronların pozitif yüklü çekirdek etrafındaki hareketini de açıklamada yetersiz kalıyordu.
Bohr Atom Modeli
Rutherford’un çalışmasından sadece iki yıl sonra 1913 yılında Niels Bohr, Rutherford’un çalışmalarından faydalanarak kendi geliştirdiği atom modelini ortaya koymuştur. Bohr atom modelinde, Rutherford’un çalışmalarını geliştirerek elektronların çekirdek etrafında birden fazla farklı yörüngede döndüğünü belirtmiştir. Elektronların sahip oldukları enerji seviyesine göre bu farklı yörüngelere yerleştiğini savunmuştur.
Bohr atom modeli, güncel atom modeline en yakın modeldir ancak bu onun tamamen doğru olduğunu göstermez. Bohr tarafından geliştirilen model hidrojen benzeri basit yapıdaki atomlar için doğru görünüyordu ancak atom yapısı karmaşık hale geldikçe hatalı davranıyordu. Elektronların hareketi ve davranışları konusunda da yetersizdir. Ancak Niels Bohr’un çalışmaları, güncel atom modelinin temellerini oluşturmuştur.
Güncel Atom Modeli
 Erwin Schrödinger'in 1926’da ortaya koyduğu ve kuantum mekanik modeli olarak da bilinen modeli o zamana kadar geliştirilen tüm modellerin eksik kalan yönlerine dair birer yanıta sahipti. Bohr’un geliştirdiği modelin eksikliklerini tamamlayan bu model elektronların yörüngelere yerleşimini açıklamıştır.
Erwin Schrödinger'in 1926’da ortaya koyduğu ve kuantum mekanik modeli olarak da bilinen modeli o zamana kadar geliştirilen tüm modellerin eksik kalan yönlerine dair birer yanıta sahipti. Bohr’un geliştirdiği modelin eksikliklerini tamamlayan bu model elektronların yörüngelere yerleşimini açıklamıştır.
Elektronların dalga karakterine sahip olduğunun ortaya koyulduğu modelde, elektronların elektron dalga boyunun tamsayı katlarında olan yörüngelere yerleşebildiği öne sürülmüştür. Bu modele göre elektronların yeri tam olarak bilinemeyeceğinden dolayı çekirdek etrafında hareket eden bir elektron bulutundan söz edilmiştir.
Takip edilen yıllarda gerçekleşen bilimsel keşifler neticesinde atomaltı parçacıklar olan kuarklar ve leptonlar hakkında kapsamlı bilgiler elde edilmiştir. Kuantum mekaniği alanında gerçekleşen çalışmalar neticesinde bu atomaltı parçacıklarında sicim adı verilen daha küçük parçalardan oluştuğu düşünülmektedir.
Günümüzde Atom ile İlgili Çalışmalar
Atom ile ilgili yürütülen çalışmalar evreni daha iyi anlamamızı sağlarken günlük hayatta da çeşitli uygulamaların ortaya çıkmasını sağlamıştır. İnsanlığında uzun yıllar boyunca maddenin parçalanamaz temel yapı taşı olarak adlandırıldığı atom çekirdeklerinin parçalanabildiği veya başka bir çekirdek ile birleşebildiği ortaya çıkmıştır.
İki elementin nükleer reaksiyonlar sonucu birleşerek daha ağır bir element oluşturması nükleer füzyon olarak adlandırılır. Güneşte ve yıldızlarda doğal olarak gerçekleşen nükleer füzyon tepkimeleri bu gök cisimlerinin temel enerji kaynağıdır. Bilim insanları bu tepkimeleri yapay olarak gerçekleştirerek enerji elde etmeyi amaçlamaktadır.
Atomun çekirdeğinin parçalanması ise nükleer fisyon tepkimesidir. Büyük kütleli atom çekirdekleri parçalanarak daha küçük çekirdekler meydana gelir ve farklı atomlar meydana çıkar. Bu işlem sırasında muazzam düzeyde enerji açığa çıkar. Nükleer enerji veya atom enerjisi santrallerinde ve Robert Oppenheimer liderliğinde geliştirilen atom bombalarında kullanılan da fisyon tepkimeleridir.
Nükleer fiziğin yanı sıra atomlar nanoteknoloji ve moleküler biyolojinin de temellerini oluşturur. Nanoteknoloji, maddeleri nano ölçekte inceleyen atom ve molekülleri manipüle ederek yeni özelliklerini değiştirme üzerine çalışır. Moleküler biyoloji ve genetik alanında yürütülen çalışmalarda ise hücreleri oluşturan moleküler yapının anlaşılması amaçlayan biyoloji dalıdır.

Evrenin yapısını öğrenme ve atomlar hakkında daha fazla bilgi edinmek amacıyla parçacık hızlandırıcıları kullanan bir dizi çalışma yürütülmektedir. Bunların dışında atomlar hakkında bildiklerimiz nanoteknoloji alanında gelişmeleri ve nano düzeyde görüntüleme ve malzeme işlemeyi mümkün hale getiren atomik kuvvet mikroskoplarının geliştirilmesini sağlamıştır. Moleküler biyoloji alanındaki çalışmalar ile canlı organizmaların yapısı ve çalışma mantığı hakkında bilgi edinilmiştir. Atom etrafındaki tüm bu çalışmalar, medeniyetin gelişmesini ve insan ömrünün uzamasının temelini oluşturur. Günlük hayatta enerji üretiminden, tıbbi görüntüleme ve tedavilere, gıda üretimi gibi pek çok farklı alanda bu bilimsel araştırmaların etkilerini görürüz.
Mikroskoplarla dahi görüntülenmesi güç boyutlardaki bir ölçekte atomlar ve atom altı parçacıklarının davranışları sizce de merak ve hayranlık uyandırıcı değil mi? Bu konu hakkındaki görüşlerinizi yorumlarda paylaşmayı unutmayın.

 Online İşlemler
Online İşlemler Başvuru Sorgula
Başvuru Sorgula Güvence Bedeli Öde
Güvence Bedeli Öde Tesisat Numarası Sorgula
Tesisat Numarası Sorgula Tazminat Bedeli Sorgula
Tazminat Bedeli Sorgula Otomatik Ödeme Talimatı Sorgula
Otomatik Ödeme Talimatı Sorgula İş Ortaklığı Başvurusu Yap
İş Ortaklığı Başvurusu Yap







Yorum Yap